
NEWS
最新消息
FDA批准长效版依库丽单抗-Ravulizumab
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2019-02-24 23:10
- 访问量:
【概要描述】2018年12月21日,FDA批准AlexionPharmaceuticals公司开发的新药ULTOMIRIS(Ravulizumab)上市,用于治疗阵发性睡眠性血红蛋白尿(PNH),该药是第一款长效C5补体抑制剂。FDA原定在2019年2月18日之前对ULTOMIRIS的申请做出决定,这一批准比预计时间提前了两个月。过去,罕见病药物依库珠单抗(商品名Soliris)用于治疗阵发性夜间血红蛋白尿症
FDA批准长效版依库丽单抗-Ravulizumab
【概要描述】2018年12月21日,FDA批准AlexionPharmaceuticals公司开发的新药ULTOMIRIS(Ravulizumab)上市,用于治疗阵发性睡眠性血红蛋白尿(PNH),该药是第一款长效C5补体抑制剂。FDA原定在2019年2月18日之前对ULTOMIRIS的申请做出决定,这一批准比预计时间提前了两个月。过去,罕见病药物依库珠单抗(商品名Soliris)用于治疗阵发性夜间血红蛋白尿症
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2019-02-24 23:10
- 访问量:
2018年12月21日,FDA批准Alexion Pharmaceuticals公司开发的新药ULTOMIRIS(Ravulizumab)上市,用于治疗阵发性睡眠性血红蛋白尿(PNH),该药是第一款长效C5补体抑制剂。FDA原定在2019年2月18日之前对ULTOMIRIS的申请做出决定,这一批准比预计时间提前了两个月。
过去,罕见病药物依库珠单抗(商品名Soliris)用于治疗阵发性夜间血红蛋白尿症(PNH)、非典型溶血性尿毒症综合征(aHUS)和抗AchR抗体阳性重症肌无力(gMG)。依库珠单抗2007年首次在美国上市,2018年09月04日在中国获批,其美国专利将于2027年到期,而ULTOMIRIS的成功上市有望将专利延长至2035年。
阵发性夜间血红蛋白尿症(PNH)
阵发性夜间血红蛋白尿症(paroxysmal nocturnal hemoglobinuria, PNH)是一种以补体介导的红细胞破坏(溶血)为特征的罕见血液疾病,由于1个或多个造血干细胞经获得性体细胞PIG-A基因(phosphotidyl inositol glycan complementation group A)突变造成的非恶性的克隆性疾病,PIG-A突变造成糖基磷脂酰肌醇(glycosyl phosphatidyl inositol,GPI)合成异常,导致由GPI锚接在细胞膜上的一组膜蛋白丢失,包括CD16、CD55、CD59等,临床上主要表现为慢性血管内溶血、再生障碍性贫血和反复血栓形成,可引起广泛的衰弱症状和并发症,该病可发生在全身,并导致器官损伤和过早死亡。
长效版依库丽单抗- Ravulizumab
英文名:Ravulizumab
商品名:ULTOMIRISTM
Ravulizumab(ALXN1210)是第一款也是目前唯一一款长效型补体抑制剂,它通过抑制终末补体级联反应中的C5蛋白从而防止溶血的发生;C5蛋白是人体免疫系统的一部分,当它不受控制被激活时,会引发PNH、溶血尿毒综合征(aHUS)、抗乙酰胆碱受体(AchR)和抗体阳性重症肌无力等严重罕见病。
在PNH适应症的临床试验中,Ravulizumab与Soliris相比具有非劣性(所有p < 0.0006),PNH患者从每2周用一次依库丽单抗转为每8周用一次Ravulizumab,效果不减,尤其是Ravulizumab正在开发皮下注射制剂,这对Ravulizumab来说具有市场发展潜力。
除已获批的PNH适应症外,Ravulizumab目前也在进行用于溶血尿毒综合征的三期临床试验。另外,针对治疗重症肌无力和皮下注射可行性的临床试验也计划启动。
专利信息
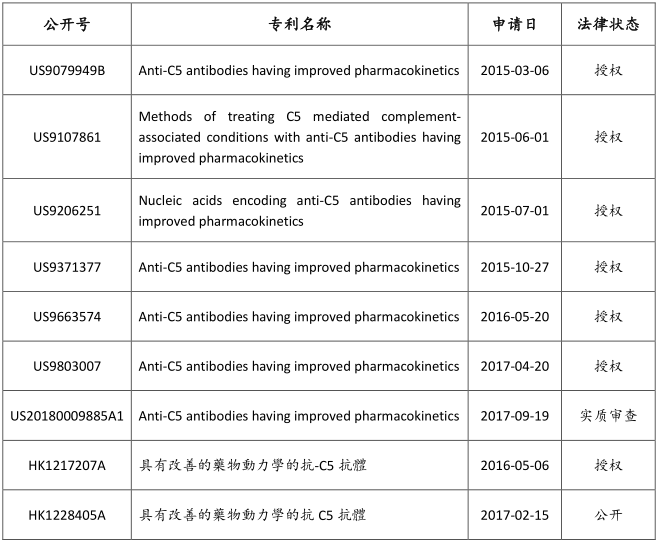
通过检索发现有7篇相关的美国专利和2篇中国同族专利,其中各有1篇专利还未授权。专利中包含通过Fc段基因工程改造提高Fc-FcRn在PH 6.0下的亲和力,延长了抗体半衰期的基因工程方案。


专利对于药厂的重要性

如何通过国知局转交的方式进行外观设计国际申请

美国联邦巡回上诉法院表示娇生公司 全球畅销精神分裂症药物的专利可能无效










