
NEWS
最新消息
恒瑞更改瑞马唑仑盐型获得I类新药
- 分类:最新消息
- 作者:
- 来源:
- 发布时间:2018-09-28 11:21
- 访问量:
【概要描述】化合物结构最终以盐型状态上市,往往可以改善药物游离状态下部分理化性质数据,这也是大多数创新药物研发工作的一部分,但在已发表的化合物的基础上,仅仅通过更改盐型即得到一个I类新药,并已发展到国内NDA阶段,这样的例子实在不多见,毕竟原研公司遗漏一个更优的盐型是不太可能的。然而就是这样的极小概率事件,恒瑞抓住了,这个产品就是当前处于NDA阶段并获得国内优先审评资格的甲苯磺酸瑞马唑仑。
恒瑞更改瑞马唑仑盐型获得I类新药
【概要描述】化合物结构最终以盐型状态上市,往往可以改善药物游离状态下部分理化性质数据,这也是大多数创新药物研发工作的一部分,但在已发表的化合物的基础上,仅仅通过更改盐型即得到一个I类新药,并已发展到国内NDA阶段,这样的例子实在不多见,毕竟原研公司遗漏一个更优的盐型是不太可能的。然而就是这样的极小概率事件,恒瑞抓住了,这个产品就是当前处于NDA阶段并获得国内优先审评资格的甲苯磺酸瑞马唑仑。
- 分类:最新消息
- 作者:
- 来源:
- 发布时间:2018-09-28 11:21
- 访问量:
化合物结构最终以盐型状态上市,往往可以改善药物游离状态下部分理化性质数据,这也是大多数创新药物研发工作的一部分,但在已发表的化合物的基础上,仅仅通过更改盐型即得到一个I类新药,并已发展到国内NDA阶段,这样的例子实在不多见,毕竟原研公司遗漏一个更优的盐型是不太可能的。然而就是这样的极小概率事件,恒瑞抓住了,这个产品就是当前处于NDA阶段并获得国内优先审评资格的甲苯磺酸瑞马唑仑。
甲苯磺酸瑞马唑仑简介
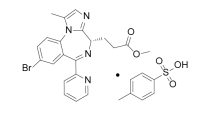
瑞马唑仑是由德国Paion公司开发的一种短效GABAa受体激动剂,是苯二氮卓类中枢神经系统药物。甲苯磺酸瑞马唑仑则是江苏恒瑞研发的瑞马唑仑成盐化合物,相比瑞马唑仑具有更高的稳定性,目前已经在中国提交上市申请,用于患者的静脉麻醉、镜检时镇痛、术前麻醉和ICU镇静。
同靶点药物现况
甲苯磺酸瑞马唑仑同靶点上市药物已达到74个,NDA申请状态3个,临床III期品种11个,临床II期品种15个,临床I期品种27个,撤市药物4个(分别为复方盐酸阿米替林/氯氮䓬、丁巴比妥、阿吡坦、甲喹酮)。临床状态方面,处于进行中的24项,无进展10项,终止28项。
中国I类新药方面,研发最为靠前的即为江苏恒瑞的甲苯磺酸瑞马唑仑。紧随其后的III期临床产品分别为Paion Pharma/宜昌人福药业的苯磺酸瑞马唑仑、海思科的HSK-3486;II期临床产品为D-Pharm/江苏恩华药业DP-VPA;I期临床产品分别为苏州沪云的SPT-07A 、苏州旺山旺水生物医药/中国科学院上海药物研究所/上海特化医药科技的TPN102。
甲苯磺酸瑞马唑仑在中国的进程
2012年6月,食药监总局承办恒瑞递交的1类新药临床申请(IND)。
2013年4月,甲苯磺酸瑞马唑仑获得中国化药1.1类临床批件。
2013年10月,甲苯磺酸瑞马唑仑临床I期研究启动。
2017年5月,甲苯磺酸瑞马唑仑获CFDA批准,进入Ⅲ期临床。
2018年3月,甲苯磺酸瑞马唑仑在中国申报生产。
2018年4月,据总局《关于鼓励药品创新实行优先审评审批的意见》(食药监药化管〔2017〕126号),CDE组织专家对申请优先审评的药品注册申请进行了审核论证,江苏恒瑞的甲苯磺酸瑞马唑仑入选理由为“与现有治疗手段相比具有明显治疗优势”。
药理、临床信息情况
江苏恒瑞对于产品甲苯磺酸瑞马唑仑的信息披露相对不多,其临床适应症主要针对胃镜、结肠镜的镇静麻醉,而从原研瑞马唑仑的相关报道中可知,瑞马唑仑是结合了咪达唑仑的安全性与异丙酚(丙泊酚)的有效性,但游离碱稳定性较差,成药性不高,而江苏恒瑞在瑞马唑仑的基础上,使用甲苯磺酸盐,而非原研公司的苯磺酸盐,毒性相对降低,故相对而言,临床安全性更高。
总结
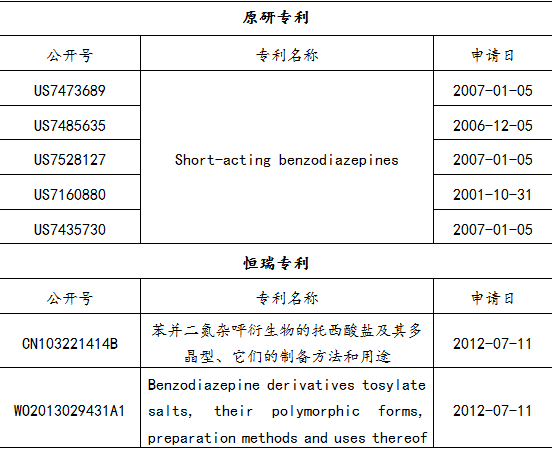
从长远的角度来看,甲苯磺酸瑞马唑仑的上市将成为恒瑞医药新的业绩增长引擎,开拓恒瑞在静脉全身麻醉领域的战略性布局,带动在研产品管线中储备药物的成长,结合恒瑞在吸入性麻醉药物领域的优势,整合静脉/吸入麻醉的整个产品管线,这是一款具有开拓性意义的药物。尽管如此,甲苯磺酸瑞马唑仑这样一个没有化合物专利的“新药”,仅仅凭借盐型专利作为第一道防线,强仿似乎不难,当然,也有可能是因为拥有着强大的销售能力以及麻醉市场占比状态,恒瑞并不担心产品的未来走势以及对手的竞争,接下来能否获批以及未来之路如何,值得大家持续关注。


专利对于药厂的重要性

如何通过国知局转交的方式进行外观设计国际申请

美国联邦巡回上诉法院表示娇生公司 全球畅销精神分裂症药物的专利可能无效










