NEWS
最新消息
首个治疗IBS-C的药物利那洛肽在中国获批
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2019-02-15 12:01
- 访问量:
【概要描述】阿斯利康公司于2019年1月15日宣布,国家药品监督管理局(NMPA)已正式批准全球第一个(Firstinclass)鸟苷酸环化酶激动剂Linzess(linaclotide,利那洛肽)在中国上市,作为我国专门治疗成人便秘型肠易激综合征(IBS-C)的处方药物。2012年8月,利那洛肽经FDA批准用于IBS-C和慢性特发性便秘患者的治疗,商品名为Linzess,该药物是全球首个获批用于便秘治疗的鸟
首个治疗IBS-C的药物利那洛肽在中国获批
【概要描述】阿斯利康公司于2019年1月15日宣布,国家药品监督管理局(NMPA)已正式批准全球第一个(Firstinclass)鸟苷酸环化酶激动剂Linzess(linaclotide,利那洛肽)在中国上市,作为我国专门治疗成人便秘型肠易激综合征(IBS-C)的处方药物。2012年8月,利那洛肽经FDA批准用于IBS-C和慢性特发性便秘患者的治疗,商品名为Linzess,该药物是全球首个获批用于便秘治疗的鸟
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2019-02-15 12:01
- 访问量:
阿斯利康公司于2019年1月15日宣布,国家药品监督管理局(NMPA)已正式批准全球第一个(First in class)鸟苷酸环化酶激动剂Linzess(linaclotide, 利那洛肽)在中国上市,作为我国专门治疗成人便秘型肠易激综合征(IBS-C)的处方药物。
2012年8月,利那洛肽经FDA批准用于IBS-C和慢性特发性便秘患者的治疗,商品名为Linzess,该药物是全球首个获批用于便秘治疗的鸟苷酸环化酶C激动剂;此外,2017年2月,FDA批准72μg的利那洛肽用于慢性特发性便秘(CIC)成人患者的治疗。在日本市场,Linzess于2016年12月获批,成为治疗IBS-C的首个处方药,并于2017年3月在日本上市。
截至目前,利那洛肽已经在全球30多个国家获批上市,成为全球IBS-C治疗领域的领先处方药。
便秘型肠易激综合征(Irritable Bowel Syndrome with Constipation, IBS-C)
肠易激综合征(IBS)是一种常见的临床功能性肠病,便秘型肠易激综合征(IBS-C)是亚型之一,临床症状主要表现为反复发作的便秘,并伴随与排便有关的腹痛、腹胀和腹部不适症状,因其反复发作,患者生存质量受到影响。
在中国,IBS的患病率高达6.5%,其中15%为IBS-C,据估计目前国内这种类型的患者群体约为1400万。然而,在利那洛肽国内上市之前,IBS-C患者的治疗主要是根据症状选择诸如解痉剂、渗透性泻药等类型的药物,国内一直缺乏针对性的有效治疗药物,此次利那洛肽在国内的获批将为中国医生及广大的患者带来全新和有效的治疗选择,填补我国成人IBS-C治疗领域的空白。
慢性特发性便秘(Chronic Idiopathic Constipation, CIC)
慢性功能性便秘是一组多人群发病、多因素存在,以排便困难、排便不适感及排便时程延长为主要症状的症候群,依病因可分为原发性(特发性)便秘和继发性便秘,其中特发性便秘由于病因不清,治疗又困难,因此又称为“难治性”或“原发性”。CIC与IBS-C类似,两者之间临床症状经常重叠,主要通过腹部症状来区别,IBS-C腹部疼痛症状不因排便而缓解。
据统计,IBS全球发病率约为11%,CIC约为14%,两者发病机制均较复杂,虽然一般不认为其与某些严重疾病或者更高的死亡率相关,但却严重影响患者的生活质量。
药物简介
中文名:利那洛肽
英文名:Linaclotide
商品名:令泽舒®(Linzess®)

利那洛肽是一种鸟苷酸环化酶-C(GC-C)激动剂,结构为含14个氨基酸的多肽,能够结合并局部作用于小肠上皮细胞的GC-C受体,GC-C的激活导致细胞内和细胞外环磷酸鸟苷(cGMP)浓度均升高,细胞内cGMP升高刺激氯离子和碳酸氢根离子分泌进入肠腔,导致小肠分泌液增加和加速通过。在动物模型中,利那洛肽还表现出减轻小肠疼痛的作用,而这被认为是细胞外cGMP增加所介导,降低了肠道疼痛感应神经的活动从而诱导内脏疼痛减轻。
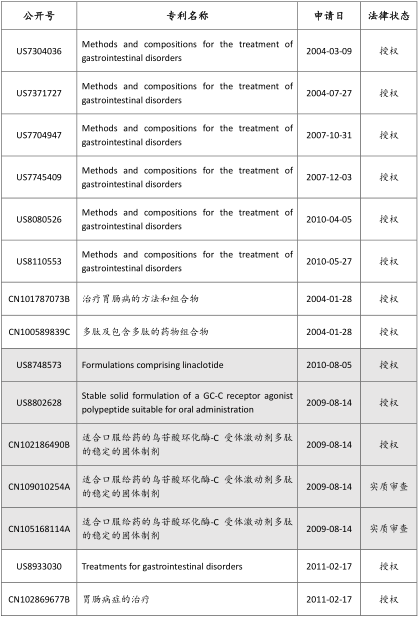
专利信息
利那洛肽在美国橙皮书中共登记有10篇相关的美国专利,有7篇中国同族专利,美国所有专利皆已授权,中国则有两篇专利还在实质审查的阶段。