
NEWS
最新消息
首款中国自主研发「维迪西妥单抗」获批
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2021-06-11 14:22
- 访问量:
【概要描述】6月9日,中国国家药监局(NMPA)宣布,已批准荣昌生物注射用维迪西妥单抗(商品名:爱地希)上市,用于治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者。该药本次获批意味着,国内首款自主研发的HER2 ADC正式由幕后走向台前,预计其可充分享受先发优势,快速抢占晚期胃癌市场。 维迪西妥单抗(disitamab vedotin,RC48)是荣昌生物开发的一款靶向HER2的抗体药物偶联物。它的分子结构包括一个新型人源化HER2抗体,其连接子在肿瘤细胞具有可裂解性,其小分子细胞毒药物具有高毒性及旁杀伤效应。根据荣昌生物新闻稿,维迪西妥单抗的抗体成分是崭新的药物,具有差异化的生物特性。该候选药能以肿瘤表面的HER2蛋白为靶点,精准识别癌细胞、穿透细胞膜,进而利用小分子细胞毒药物将其杀死。 在中国,维迪西妥单抗的新药上市申请于2020年8月获得中国国家药监局药品审评中心(CDE)受理,并因“符合附条件批准的药品”被纳入优先审评。 据悉,维迪西妥单抗在中国提交的胃癌上市申请是基于一项2期注册性临床试验数据。在该研究中,维迪西妥单抗表现出优异的抗肿瘤活性和良好耐受性。除了胃癌,维迪西妥单抗目前正在中国进行尿路上皮癌、HER2低表达乳腺癌,以及肺癌和胆管癌等的临床研究。其中,维迪西妥单抗针对HER2过表达局部晚期或转移性尿路上皮癌患者的申请,已于2020年12月被CDE纳入突破性治疗品种。 在2021年的ASCO大会上,荣昌生物公布了维迪西妥单抗的多项临床研究最新数据。一项1b/2期研究初步结果显示:维迪西妥单抗联合抗PD-1单抗特瑞普利单抗一线治疗转移性尿路上皮癌,在有不同程度HER2表达的16个患者中,客观缓解率(ORR)达到100%。而另一项针对乳腺癌患者的研究也显示,维迪西妥单抗对HER2低表达乳腺癌患者也取得了良好疗效。 目前,荣昌生物正在全球范围内探索维迪西妥单抗的疗效。在美国,FDA已授予维迪西妥单抗快速通道资格,针对适应症为晚期或转移性胃癌以及胃食管结合部腺癌。此外,该药治疗尿路上皮癌的申请也获得了FDA的突破性疗法认定和快速通道资格。 期待这款抗体药物偶联物早日来到患者身边,为他们带来新的治疗选择。
首款中国自主研发「维迪西妥单抗」获批
【概要描述】6月9日,中国国家药监局(NMPA)宣布,已批准荣昌生物注射用维迪西妥单抗(商品名:爱地希)上市,用于治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者。该药本次获批意味着,国内首款自主研发的HER2 ADC正式由幕后走向台前,预计其可充分享受先发优势,快速抢占晚期胃癌市场。
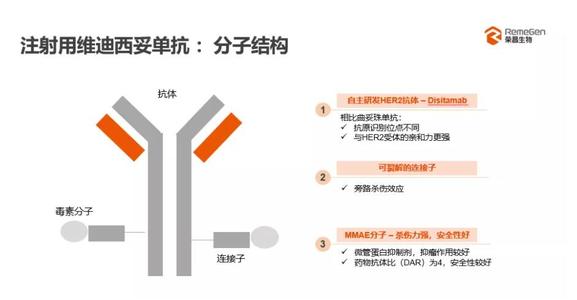
维迪西妥单抗(disitamab vedotin,RC48)是荣昌生物开发的一款靶向HER2的抗体药物偶联物。它的分子结构包括一个新型人源化HER2抗体,其连接子在肿瘤细胞具有可裂解性,其小分子细胞毒药物具有高毒性及旁杀伤效应。根据荣昌生物新闻稿,维迪西妥单抗的抗体成分是崭新的药物,具有差异化的生物特性。该候选药能以肿瘤表面的HER2蛋白为靶点,精准识别癌细胞、穿透细胞膜,进而利用小分子细胞毒药物将其杀死。
在中国,维迪西妥单抗的新药上市申请于2020年8月获得中国国家药监局药品审评中心(CDE)受理,并因“符合附条件批准的药品”被纳入优先审评。
据悉,维迪西妥单抗在中国提交的胃癌上市申请是基于一项2期注册性临床试验数据。在该研究中,维迪西妥单抗表现出优异的抗肿瘤活性和良好耐受性。除了胃癌,维迪西妥单抗目前正在中国进行尿路上皮癌、HER2低表达乳腺癌,以及肺癌和胆管癌等的临床研究。其中,维迪西妥单抗针对HER2过表达局部晚期或转移性尿路上皮癌患者的申请,已于2020年12月被CDE纳入突破性治疗品种。
在2021年的ASCO大会上,荣昌生物公布了维迪西妥单抗的多项临床研究最新数据。一项1b/2期研究初步结果显示:维迪西妥单抗联合抗PD-1单抗特瑞普利单抗一线治疗转移性尿路上皮癌,在有不同程度HER2表达的16个患者中,客观缓解率(ORR)达到100%。而另一项针对乳腺癌患者的研究也显示,维迪西妥单抗对HER2低表达乳腺癌患者也取得了良好疗效。
目前,荣昌生物正在全球范围内探索维迪西妥单抗的疗效。在美国,FDA已授予维迪西妥单抗快速通道资格,针对适应症为晚期或转移性胃癌以及胃食管结合部腺癌。此外,该药治疗尿路上皮癌的申请也获得了FDA的突破性疗法认定和快速通道资格。
期待这款抗体药物偶联物早日来到患者身边,为他们带来新的治疗选择。
- 分类:最新消息
- 作者:华讯知识产权
- 来源:
- 发布时间:2021-06-11 14:22
- 访问量:
6月9日,中国国家药监局(NMPA)宣布,已批准荣昌生物注射用维迪西妥单抗(商品名:爱地希)上市,用于治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者。该药本次获批意味着,国内首款自主研发的HER2 ADC正式由幕后走向台前,预计其可充分享受先发优势,快速抢占晚期胃癌市场。

维迪西妥单抗(disitamab vedotin,RC48)是荣昌生物开发的一款靶向HER2的抗体药物偶联物。它的分子结构包括一个新型人源化HER2抗体,其连接子在肿瘤细胞具有可裂解性,其小分子细胞毒药物具有高毒性及旁杀伤效应。根据荣昌生物新闻稿,维迪西妥单抗的抗体成分是崭新的药物,具有差异化的生物特性。该候选药能以肿瘤表面的HER2蛋白为靶点,精准识别癌细胞、穿透细胞膜,进而利用小分子细胞毒药物将其杀死。
在中国,维迪西妥单抗的新药上市申请于2020年8月获得中国国家药监局药品审评中心(CDE)受理,并因“符合附条件批准的药品”被纳入优先审评。
据悉,维迪西妥单抗在中国提交的胃癌上市申请是基于一项2期注册性临床试验数据。在该研究中,维迪西妥单抗表现出优异的抗肿瘤活性和良好耐受性。除了胃癌,维迪西妥单抗目前正在中国进行尿路上皮癌、HER2低表达乳腺癌,以及肺癌和胆管癌等的临床研究。其中,维迪西妥单抗针对HER2过表达局部晚期或转移性尿路上皮癌患者的申请,已于2020年12月被CDE纳入突破性治疗品种。
在2021年的ASCO大会上,荣昌生物公布了维迪西妥单抗的多项临床研究最新数据。一项1b/2期研究初步结果显示:维迪西妥单抗联合抗PD-1单抗特瑞普利单抗一线治疗转移性尿路上皮癌,在有不同程度HER2表达的16个患者中,客观缓解率(ORR)达到100%。而另一项针对乳腺癌患者的研究也显示,维迪西妥单抗对HER2低表达乳腺癌患者也取得了良好疗效。

目前,荣昌生物正在全球范围内探索维迪西妥单抗的疗效。在美国,FDA已授予维迪西妥单抗快速通道资格,针对适应症为晚期或转移性胃癌以及胃食管结合部腺癌。此外,该药治疗尿路上皮癌的申请也获得了FDA的突破性疗法认定和快速通道资格。
期待这款抗体药物偶联物早日来到患者身边,为他们带来新的治疗选择。


美国联邦巡回上诉法院表示娇生公司 全球畅销精神分裂症药物的专利可能无效

注射用醋酸地加瑞克专利无效口审将于本月底进行

外观专利如何进行海外布局?










